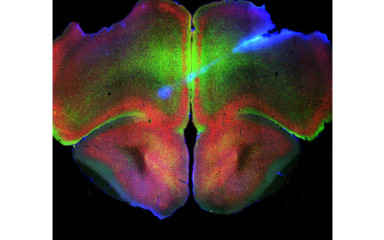
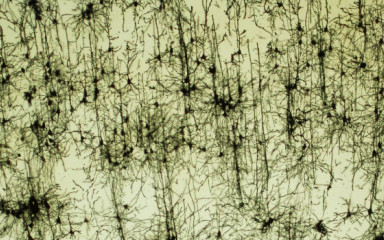
Stressz és félelmi reakciók neurobiológiai alapjai és kóros elváltozásai
A mentális betegségek összköltsége, amelyek közül a szorongásos, depressziós rendellenességek a legelterjedtebbek, meghaladhatja az évi 600 milliárd eurót (OECD 2018). A COVID-19 világjárvány következtében tapasztalható, drámaian növekvő esetszám a korábbinál is sürgetőbb feladattá tette hatékony kezelési módok fejlesztését. Az elmúlt évtizedek kutatásai számos részsikert tudnak felmutatni mind a stresszel összefüggő betegségek, mind a szorongás és a depresszió kezelésében, de hatékony terápiás megoldások eddig még nem születtek.
A pszichés stresszorok komplex hormonális, vegetatív és viselkedési válaszreakciókat váltanak ki, melyeket a központi idegrendszer koordinál. Ha sikeres a stratégia az adott provokációra, a stresszválasz lecseng és a válasz olyan emléknyomok formájában rögzül, amely segíti a szervezet hozzászokását (habituáció) az adott kihíváshoz. Ha a megküzdés nem eredményes vagy nem lehetséges, az újabb stresszorok előhívják a stresszel kapcsolatos emlék-képeket, a stresszválasz és a félelem felerősödik Abban az esetben, amikor a megküzdés ismételten eredménytelen, vagy a szervezet védekező mechanizmusai kimerültek, kialakul a depresszió.
A WHO előrejelzése szerint 2030-ra a világ legnagyobb egészségügyi-gazdasági terhet jelentő betegsége a depresszió less. A kezelés szempontjából alapvető, hogy a megfelelően diagnosztizált embereket a lehető leghamarabb, a számukra leghatékonyabb terápiával kezeljük. Az ilyen terápiák kidolgozásához pedig elengedhetetlen az elváltozásokat okozó idegrendszeri mechanizmusok pontos ismerete.
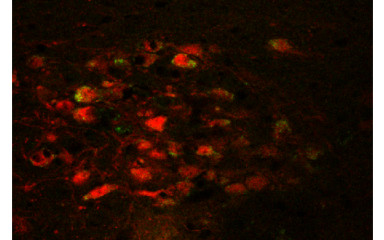
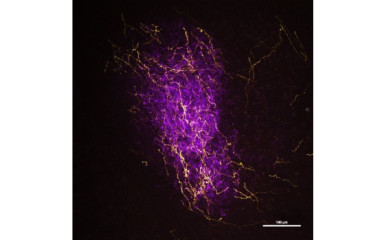
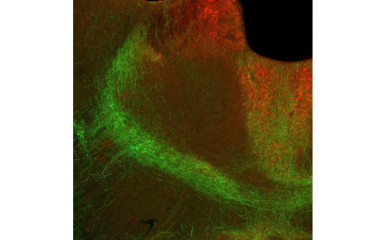
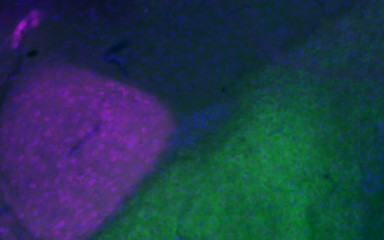
Az intézetben folyó célzott, stratégiai kutatások hozzájárulnak hatékony terápiás eljárások fejlesztéséhez a transzlációs, preklinikai modelleken, legmodernebb neuroanatómiai, genetikai, idegélettani és magatartási vizsgáló módszerekkel, a stressz válasz és a kóros félelmi reakciók számos aspektusát célzó vizsgálataival.